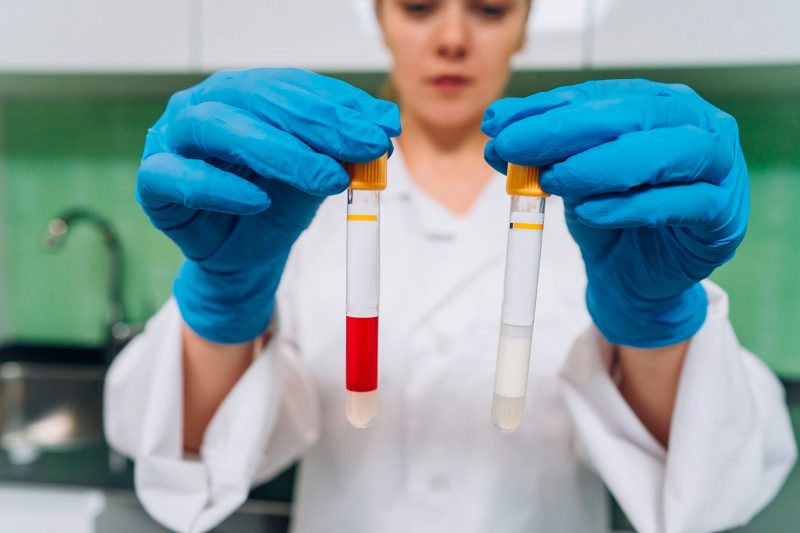
En estos tiempos que nos vemos envueltos en la pandemia del COVID-19, en todos los medios de comunicación se tratan los ensayos clínicos para conseguir una vacuna preventiva para el coronavirus.
En este orden, los ensayos clínicos son una de las grandes esperanzas de los pacientes con enfermedades poco frecuentes, ya que les permite acceder en fases tempranas a medicamentos innovadores.
Sin embargo, debido a la situación sanitaria actual, el manejo de los ensayos clínicos también se ha visto afectado. En cualquier caso, la nueva gestión de estos estudios no debe suponer una merma en los derechos de los pacientes, ni evidentemente, una reducción de los niveles de seguridad de dichos ensayos, especialmente en una población que es particularmente vulnerable a los efectos del virus y por razón de sus propias patologías, normalmente graves y muy discapacitantes. Ante esta preocupación las autoridades sanitarias, tanto europeas como nacionales han establecido directrices al respecto.
Naturalmente, la primera consideración a tener presente en los ensayos clínicos, en este y cualquier otro momento, es la seguridad del paciente y el impacto en su salud, debiendo ser objeto de supervisión médica continua, en este caso preferiblemente de manera telemática, a través de contacto telefónico o implementando canales de asistencia mediante telemedicina, en caso de que por razones de distanciamiento no se pueda realizar el seguimiento en las condiciones habituales. En todo caso, en aquellos supuestos en los que sea ineludible la presencia física del paciente, se deberá tener en consideración la habilitación de zonas limpias y seguras de los centros sanitarios, garantizando, por encima de todo la seguridad de la persona participante en el ensayo.
Se debe garantizar el acceso de los pacientes a la medicación del ensayo en las mismas condiciones en las que se estaba suministrando anteriormente. En este sentido sería conveniente que se reciba una cantidad de medicamento que permita cubrir un periodo mayor de tratamiento en el caso de que el paciente acuda a una visita programada. En el caso de que se realice seguimiento a distancia, sería perentorio la dispensación a domicilio de la medicación, estableciendo los mecanismos de seguridad necesarios en cuanto a la privacidad, confidencialidad y protección de los datos de los pacientes.
En este sentido, el Ministerio de Sanidad ha habilitado la dispensación domiciliaria de medicamentos hospitalarios y de medicamentos en ensayo clínico, a través de la Orden SND/293/2020, de 25 de marzo, por la que se establecen condiciones a la dispensación y administración de medicamentos en el ámbito del Sistema Nacional de Salud, ante la situación de crisis sanitaria ocasionada por el COVID-19. Igualmente, a nivel de las comunidades autónomas, como competentes en la materia, ya se establecía, de manera incipiente, supuestos especiales de entrega domiciliaria de medicamentos, como son los casos de Galicia, Andalucía, Cantabria, Navarra, La Rioja, Extremadura o Valencia; mientras que en algunas CCAA en las que no existía dicha previsión legal, se están favoreciendo normativas ad hoc, como es el caso, por ejemplo, de la Comunidad de Madrid, por la que se establecen medidas relacionadas con la dispensación de medicamentos y actividades de los servicios de farmacia hospitalaria durante el estado de alarma; autorizando el establecimiento de procedimientos de atención farmacéutica no presencial con entrega de medicación a domicilio, que garantice la continuidad de la prestación farmacéutica, manteniendo todas las garantías de efectividad, seguridad y adherencia de los tratamientos, autorizando a los Servicios de Farmacia Hospitalaria y a la Sección de Medicamentos Extranjeros para que puedan entregar a domicilio la medicación cuya dispensación se realiza, de forma habitual, de manera presencial.
Se debe garantizar el acceso de los pacientes a la medicación del ensayo en las mismas condiciones en las que se estaba suministrando anteriormente
En este orden de cosas, el Tribunal Constitucional tiene avalado la dispensación farmacéutica domiciliaria a los pacientes crónicos, señalando la posibilidad de dispensar medicamentos a los enfermos de larga duración mediante servicios de mensajería sin que por ello se quebrante el núcleo de la garantía de la salud de estos pacientes, siempre que dicha dispensación respete las condiciones de prescripción, supeditando la dispensación del medicamento a su cobertura con la correspondiente orden médica.
Son muchas los requerimientos legales para la correcta llevanza de un ensayo clínico. Recordamos, de manera no exhaustiva, algunos de los aspectos que tienen relación con la situación actual, que son:
1. El ensayo clínico debe ser ética y metodológicamente correcto y debe estar diseñado para que se obtengan datos fiables y sólidos.
2. Los beneficios para el sujeto del ensayo o para la salud pública esperados justifican los riesgos y los inconvenientes previsibles, y se supervisa de forma constante el cumplimiento de esta condición. No obstante, los derechos, la seguridad, la dignidad y el bienestar de los sujetos prevalecen sobre cualquier otro interés.
3. Se obtiene y documenta el consentimiento informado de cada uno de los sujetos del ensayo, libremente expresado, antes de su inclusión en el ensayo y con los cambios necesarios durante el mismo.
4. Se respetan los derechos del sujeto a su integridad física y mental, y a su intimidad, y se protegen los datos de carácter personal que le conciernen.
5. El ensayo clínico ha sido diseñado para reducir al mínimo posible el dolor, la incomodidad, el miedo y cualquier otro riesgo previsible para los sujetos del ensayo y tanto el nivel de riesgo como el grado de incomodidad están específicamente definidos en el protocolo y bajo supervisión constante.
#todosaldrábien